O药获批成为中国首个胃癌免疫治疗药物,重振晚期胃癌治疗信心
导语:纳武利尤单抗正式开启我国胃癌免疫治疗新时代!
日前,中国第一款PD-1抑制剂纳武利尤单抗注射液(商品名:欧狄沃,又称O药)又迎来了一个重要的里程碑 —— 中国国家药品监督管理局(NMPA)正式批准其用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管连接部腺癌患者。这是纳武利尤单抗继非小细胞肺癌、头颈部鳞状细胞癌后,在中国获批的第三个适应证,标志着中国胃癌治疗正式进入免疫时代。
对于本次获批,北京大学肿瘤医院副院长、消化肿瘤内科主任沈琳教授表示:“作为第一个在中国获批用于胃癌治疗的免疫肿瘤药物,纳武利尤单抗突破了中国胃癌治疗‘后线缺药’的僵局,有望重振晚期胃癌治疗信心,具有里程碑意义。”
据悉,此次获批基于一项名为ATTRACTION-2的Ⅲ期临床研究,该研究结果明确了胃癌免疫治疗在东亚人群中的有效性及安全性,也使纳武利尤单抗成为了首个且迄今唯一经Ⅲ期临床研究证实能为中国晚期胃癌患者带来显著生存获益的PD-1抑制剂:
与对照组相比,纳武利尤单抗一年生存率翻倍,达27.3%
经纳武利尤单抗治疗缓解患者,中位生存期超2年
纳武利尤单抗不良反应发生率低且可控[
经典回“胃”
ATTRACTION-2确立胃癌免疫治疗基石地位
放眼全球胃癌数据,亚洲地区是胃癌的高发地区,亚洲胃癌发病数占全球近75%。也正是通过对亚洲患者的研究,ATTRACTION-2成为了首个确立胃癌免疫治疗的有效性与安全性的多中心III期临床试验。
ATTRACTION-2研究纳入了493位日本、韩国与中国台湾既往至少二线化疗失败或不耐受的晚期胃或胃食管连接部腺癌(G/GEJ)患者,按2:1的比例随机分为纳武利尤单抗组(n=330)和安慰剂组(n=163)。
2年随访数据显示,纳武利尤单抗相比对照组显示出显著的生存获益:
中位总生存期(OS)显著延长(5.26 个月vs 4.14个月);
死亡风险降低38%(HR 0.62,P<0.0001);
2年OS率超3倍于对照组(10.6%vs 3.2%)。
基于此,纳武利尤单抗获批成为了全球首个胃癌免疫治疗药物,早前已在日本、中国台湾、韩国、新加坡和瑞士获批用于晚期G/GEJ肿瘤三线或以上治疗。
今年1月,美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)最新公布了ATTRACTION-2研究3年随访的生存数据,这也是迄今为止胃癌三线治疗的最长随访数据。
结果显示,纳武利尤单抗治疗的“长尾效应”明显:
3年OS率近3倍于对照组(5.6% vs 1.9%);
纳武利尤单抗组和对照组分别有15例和3例患者存活时间超过3年,而对照组的3例患者中,有2例在后续接受了纳武利尤单抗治疗;
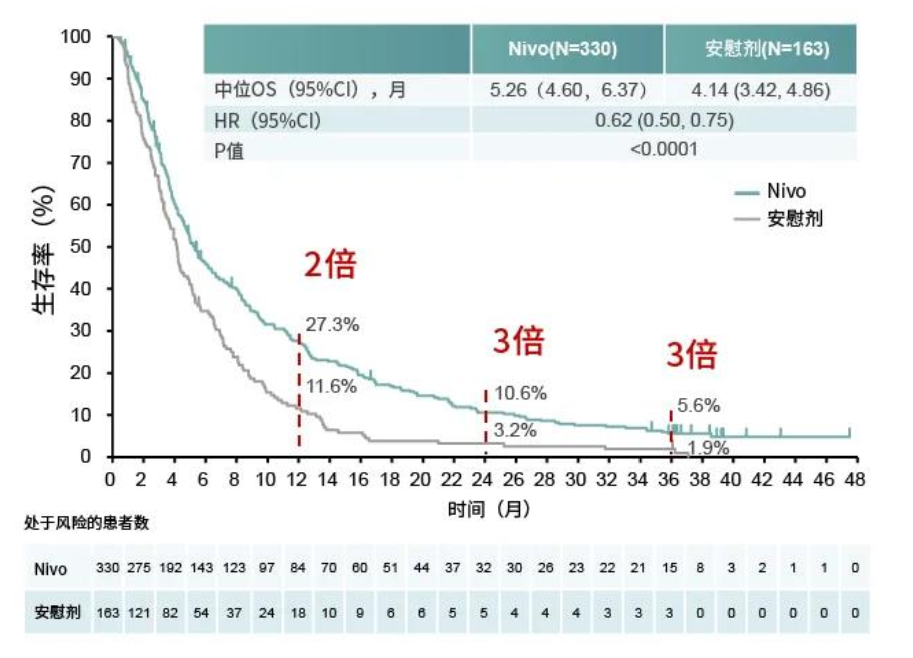
ATTRACTION-2研究3年OS率结果
此外,与对照组相比,纳武利尤单抗的无进展生存(PFS)数据优势依然明显。纳武利尤单抗组3年PFS率2.4%,对照组的值已降为0。
研究进一步根据最佳客观响应(BOR)进行OS亚组分析,纳武利尤单抗组有32位(9.7%)患者取得完全缓解(CR)/部分缓解(PR),其中位OS达到惊人的26.68个月,超过2年大关,而对照组无CR/PR。即使取得疾病稳定(SD)的患者,纳武利尤单抗组的中位OS在数值上也长于对照组(8.87 vs 7.62个月)。
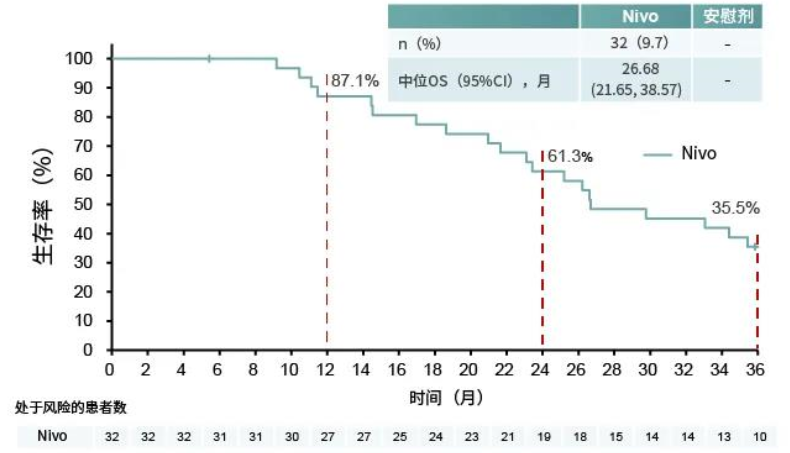
经纳武利尤单抗治疗缓解患者中位OS超过2年
安全性分析显示,大多数患者的首次治疗相关不良反应(TRAEs)发生在开始纳武利尤单抗治疗3个月内,在后续3年的随访过程中未再发现新的安全事件。
也正因此,基于ATTRACTION-2研究领衔的胃癌免疫治疗关键性数据,包含纳武利尤单抗在内的PD-1抑制剂目前已被国内外指南[2019欧洲肿瘤内科学会(ESMO)、2019 中国临床肿瘤学会(CSCO)]一致推荐成为胃癌三线治疗新标准。
中国“胃”道
O药是目前唯一经III期临床研究证实为中国人群带来生存获益的PD-1抑制剂
由于人种、环境、生活方式的不同,东西方的胃癌流行病学、治疗等方面都存在差异。
ATTRACTION-2是一项专门针对亚洲胃癌患者的免疫治疗研究,开创性地由亚洲人群入手。该研究结果明确了胃癌免疫治疗在东亚人群中的有效性及安全性,也使纳武利尤单抗成为了首个且迄今唯一经Ⅲ期临床研究证实能为中国晚期胃癌患者带来显著生存获益的PD-1抑制剂。
2019年中国临床肿瘤学会(CSCO)大会胃癌专场上,ATTRACTION-2研究的中国台湾地区亚组数据进行了口头汇报。分析数据显示,中国台湾地区亚组患者的疗效和安全性结果与ATTRACTION-2研究整体人群数据基本一致。而从死亡风险的角度比较,中国亚组数据甚至优于整体人群(OS风险比为0.49vs 0.62)。
在中国台湾患者中,纳武利尤单抗组1年OS率为20%,2年OS率为10%,而对照组则均已为0%;更值得注意的是,纳武利尤单抗组的2年中位OS也显著优于安慰剂组(5.06个月 vs 4.11个月)。
在中国台湾地区亚组患者中,纳武利尤单抗的客观缓解率(ORR)达到12.5%,包含了4.2%的CR患者比率[5];疾病控制率(DCR)亦与整体人群大体一致。此外,该亚组患者的肿瘤负荷减少比例近一半,安全性结果良好,与整体人群情况基本符合,没有新的针对中国亚组的TRAEs发现。
上下求索
期待更多用“武“之地
回望2014年,率先启动的ATTRACTION-2研究专为亚洲胃癌患者而来,在而后的近6年时间里,从东方到全球,从后线到前线,从单药到联合,在纳武利尤单抗的带领下,免疫治疗在胃癌领域的发展不断向前推进。
回首纳武利尤单抗的发展历程,自2014年7月成为全球首个获得监管机构批准的PD-1抑制剂以来,其在各个癌种中的应用已经获得了越来越多的认证。着眼未来,我们也看到,纳武利尤单抗和免疫治疗在消化道以及其他更多瘤种中的潜力正在进一步被挖掘,以造福更多的肿瘤患者。
但不可否认的是,在众多“中国特色”重大疾病问题仍尚待解决的今天,我们仍需要研究者与医患在实验室及临床去落实与发展更多的基础研究,创造更多新的可能。
据了解,目前在国内,百时美施贵宝已经开展了超过30项免疫肿瘤临床研究,其中大多数为Ⅲ期临床研究,覆盖了肝、食管、结直肠癌等多个消化道瘤种。我们可以相信,在不久的将来,这位生物制药领头人还能带领更多创新方案为消化道癌症以及中国其他特色瘤种的治疗带来一次又一次的突破!
参考文献:
[1] Chen L-T. et al. A phase 3 study of nivolumab in previously treated advanced gastric or gastroesophageal junction cancer (ATTRACTION‑2): 2‑year update data [J]. Gastric Cancer 2019(19).
[2] Kang YK, et al. Nivolumab in patients with advanced gastric or gastro-oesophageal junction cancer refractory to, or intolerant of, at least two previous chemotherapy regimens (ONO-4538-12, ATTRACTION-2): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2017 Dec 2;390(10111):2461-2471. doi: 10.1016/S0140-6736(17)31827-5. Epub 2017 Oct 6.
[3] World Health Organization International Agency for Research on Cancer Web site, Cancer Fact Sheets: Stomach Cancer. Available from:
[4] A phase III study of Nivolumab(NIVO)in previously treated advanced gastric or gastric esophageal junction(G/GEJ) cancer (ATTRACTION-2):Three-year update data. 2020ASCO GI,Abstract#383.
[5] Chao Y, Chen JS, Yeh KH, et al. Nivolumab in Advanced Gastric or Gastroesophageal Junction Cancer Refractory to, or Intolerant of, at Least Two Previous Chemotherapy Regimens: a Taiwaness Subgroup Analysis of ATTRACTION-2 Study. GEST (2019) Annual Meeting.
