Gut Microbiome在肠道芯片中设置房屋
通常,肠道内的微生物菌群足够和蔼可亲。这就是他们有资格成为共生的原因。但当他们从家中带走并带到不自然的环境中时,他们可以很快地受到欢迎。事实上,在一天之内,它们可以过度生长并杀死培养皿中的宿主人体细胞。尽管如此,肠道的微生物能够成为优秀的客人 - 并且如果它们被适当地容纳,则显示出普通的宿主 - 微生物体行为。
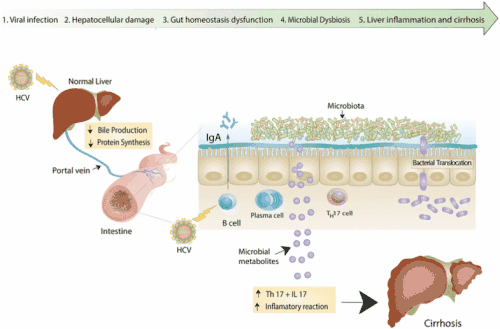
哈佛大学Wyss研究所的研究人员已经开发出一种微流体肠道芯片,即片上肠道,以显示主持人如何帮助可能令人不愉快的客人记住他们的礼仪。它可以培养稳定的复杂人类微生物组,其与血管化的人肠上皮细胞直接接触至少5天。
肠道芯片成功的关键是维持低氧条件。肠道中的许多共生微生物是厌氧的,因此它们需要非常低的氧气条件才能生长。但这些情况会伤害人体细胞。肠道芯片的设计使其能够容纳有氧和厌氧肠道微生物以及人体细胞。
5月13日,“自然生物医学工程”杂志刊登了一篇名为“在厌氧肠道中培养的复杂人体肠道微生物组”的文章。
“我们[使用]了一个微流体肠道芯片,可以控制和实时评估生理相关的氧气梯度,”该文章的作者写道。“与有氧共培养条件相比,芯片中腔内缺氧梯度的建立增加了肠道屏障功能并维持了生理相关的微生物多样性水平,包括来自11个不同属的200多个独特的操作分类单位和丰富的饲养厌氧菌,其中厚壁菌门和拟杆菌的比例与人类粪便中观察到的相似。“
我们对人体 - 微生物组相互作用的了解大多基于使用基因组或宏基因组分析的粪便样品中所含的疾病状态和细菌DNA之间的相关性研究。这是因为研究微生物组与人体外肠组织之间的直接相互作用是一项艰巨的挑战。
这种新的肠道芯片提供了一种在体外高度控制的条件下在细胞和分子水平上研究临床相关的人类宿主 - 微生物组相互作用的方法,“研究负责人Donald Ingber,医学博士,博士,Wyss研究所的创始主任说。“通过提供直接进入微生物组和分化的肠组织,这种方法可用于发现导致疾病或可能有助于预防这些疾病的特定微生物或其代谢产物,并且因为我们使用从患者分离的细胞,可以使用这种方法对于个性化医疗也是如此。“
“早期的组织培养系统不能使人类微生物组和肠上皮细胞彼此直接接触,并且它们不能模拟肠道中对于厌氧细菌存活至关重要的低氧浓度。更复杂的事情:沿着小肠向结肠行进,氧气水平不断下降,这也改变了局部微生物组组成。
对于他们的厌氧肠片,Wyss团队利用其经过验证的肠道芯片,其中包含两个由多孔膜隔开的平行微通道。它们在上部通道的膜顶部培养人肠上皮细胞,在下部通道膜的另一侧培养来自肠微血管的血管内皮细胞。用于排列这些肠道芯片的肠细胞来自细胞系或来自人体回肠活组织检查,并通过中间类器官步骤扩增,其中它们形成微小的球形肠组织结构,在培养之前将其分解成片段。芯片。
为了容纳一个完整的微生物组,该团队将肠道芯片放入定制设计的厌氧室中,这使得它们能够显着降低上肠上皮通道中的氧浓度,同时保持下部内皮通道处于正常氧浓度。“我们在两个通道上产生氧气梯度,这仍然允许肠上皮细胞通过多孔膜扩散氧气,”Ingber团队研究助理的共同第一作者Elizabeth Calamari说。
然后将从健康人粪便中获得并在无菌(gnotobiotic)小鼠中稳定培养或从婴儿粪便中新鲜分离的复杂肠道微生物组样品注射到上部上皮通道中,在那里它们与由天然分泌的粘液层直接接触。潜在的肠上皮细胞。更重要的是,当在这些低氧条件下生长时,共生细菌群体的多样性保持了在人肠中观察到的丰富性。
能够在体外和数天内观察与人体肠道组织直接接触的完整人类微生物组的组成和变化,为个性化医学和药物测试提供了机会。“我们可以培养来自同一个体的区域特异性肠组织和微生物组,以找到对特定致病,炎症和全身性疾病具有敏感性或耐受性的关联,”共同第一作者,博士后研究员Francesca Gazzaniga博士说道。 Ingber的小组和共同作者Dennis Kasper博士,哈佛医学院免疫学教授。“使用无氧肠道芯片,我们还可以测试药物对人体微生物组的直接影响,然后再将其传递给人们。”
推荐内容
-
新型靶向消炎纳米药物可控制动脉粥样硬化
布莱根妇女医院的科学家在临床前模型中进行的一项研究表明,向动脉脂肪沉积提供特殊类型的治疗分子的纳米级无人机可能成为预防由动脉粥...
-
心理咨询之婚恋观——女人都是醋坛子?法媒揭女性吃醋的4大真实原
21世纪的单身男女对于婚姻总是充满了未知和些许恐惧。好像结了婚就会失去自己的个人自由,实际情况真是如此吗?也不见得,但是现在单身...
-
无创脑刺激在内存上转回时钟
根据今天(4月8日)发表在自然 - 神经科学杂志上的一项研究,对关键大脑区域进行N次入侵刺激可以帮助人们扭转工作记忆中常见的与年龄相关的
-
不同年龄段儿童害怕对象不同
家家都有本难念的经,特别是有小孩的家庭。在和孩子相处的过程中很多家长都在不断学习,怎么跟孩子交流起来更有效,怎么不跟孩子发脾气...
-
怎样克服孩子怕黑心理
家家都有本难念的经,特别是有小孩的家庭。在和孩子相处的过程中很多家长都在不断学习,怎么跟孩子交流起来更有效,怎么不跟孩子发脾气...
-
心理咨询之婚恋观——如何让小三无机可乘_怎样保卫婚姻
现在的年轻人对于婚姻和爱情大部分是很被动的,他们觉得感情这种事随缘就好,其实一个人也可以过的很精彩。但是没经历过你又怎么知道爱...
-
如何经营好婚姻
爱情和婚姻本身是美好的东西,但是因为每个人处理的方式不同导致结果有好有坏。很多人其实可以少看一些网络案例,毕竟感情这种事是很难...
-
孤独症症状体现
孩子是祖国的未来,我们必须时刻关注青少年的身体健康和心理健康。现在社会的压力很大,如果没有一个强大的心脏是无法承受住当今社会的...
-
心理咨询之婚恋观——【如何抱怨让感情升温】3种巧抱怨让感情升温
现在的年轻人对于婚姻和爱情大部分是很被动的,他们觉得感情这种事随缘就好,其实一个人也可以过的很精彩。但是没经历过你又怎么知道爱...
-
聪明女人怎么成功击退小三
现在的年轻人对于婚姻和爱情大部分是很被动的,他们觉得感情这种事随缘就好,其实一个人也可以过的很精彩。但是没经历过你又怎么知道爱...