揭示HIV整合酶的结构告知药物的发现
在John Foundation Core中,我们依靠一系列最先进的仪器。我们使用的所有技术结合在一起并相互补充,以提供对结构和功能的更深入理解。
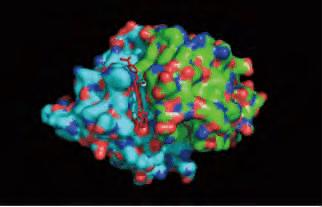
光散射测量是我们正在进行的研究的关键推动因素。事实上,我们日常工具箱中最受欢迎和最具生产力的工作是我们的光散射仪器,全部由Wyatt Technology制造。这些包括我们的Dynapro Nanostar动态光散射(DLS)仪器;我们的SEC-MALS组件,DAWN多角度光散射仪和Optilab折射率检测器与尺寸排阻色谱相结合;和我们最近的收购,我们的CG-MALS(成分 - 梯度多角度光散射)仪器,Calypso。
在过去的十年中,该团队的许多论文和资助的研究都包含了各种各样的光散射。
MALS直接测量由于生物聚合物的分子量而发生的光散射水平,使得能够独立测量其在溶液中的性质。由于两种分子(例如蛋白质和蛋白质或蛋白质和核酸)之间的大分子相互作用,质量以及因此散射光的量增加。这种现象可以像形成二聚体的两种单体一样简单,也可以像聚合和蛋白质聚集这样复杂的事件。
动态光散射(DLS)测量分子布朗运动产生的散射光强度的波动。分析信号以确定平移扩散系数,从而确定分子的大小或流体动力学半径。
DLS和MALS已成为生物大分子研究成功的日常先决条件。对于那些使用低速电子显微镜,X射线晶体学或核磁共振等从头技术的人来说,重组制剂的常规分析和批次间验证是成功确定结构的关键步骤。
对于表征重组制剂的活性和抑制的酶学家来说,批次间验证是准确发现和评估铅目标的关键。对于像我这样的小角度X射线和中子散射科学家,如果没有这些关键的实验措施,几乎不可能可靠地解释实验结果。
在过去十年中,我亲自在宾夕法尼亚州进行了数百次SEC-MALS实验,进行了广泛的研究,包括蛋白质 - 核酸相互作用,RNA剪接,HIV生物学和药物发现,蛋白质 - 蛋白质相互作用,特异性重组和染色质结构。
SEC-MALS是尺寸排阻色谱,与多角度光散射一致。在生物化学和结构生物学研究中,它是最流行的光散射实现之一。
将感兴趣的样品通过标准色谱柱以根据其大小分离大分子。然后来自该分离的洗脱液进入多角度光散射仪器,其中每秒记录多个光散射角。差示折射率检测器可用于直接确定每个时间点的大分子浓度。
然后可以从光散射和浓度数据确定分子量,而不需要任何标准曲线或理论消光系数。分析与保留时间和关于构象或柱相互作用的任何假设无关。
你能告诉我们更多关于你的艾滋病研究吗?
艾滋病毒艾滋病流行病仍然是一个重大的全球公共卫生问题,目前全世界有3700万人受到感染。预计到2020年将有3000万人服用抗逆转录病毒疗法。然而,由于对现有抗逆转录病毒药物的病毒抗性的发展阻碍了治疗工作,因此需要新的治疗方法。
FDA批准的抗HIV药物是链转移抑制剂(STI),其阻断HIV DNA整合到宿主基因组中以形成原病毒。这些化合物的最新一代现在正在优化,以抵消新出现的耐药性并改善药物的半衰期。
我的主要研究领域是HIV整合酶,其中包括催化链转移。整合酶是HIV基因组编码的三种酶之一。它是一种32千道尔顿的三结构域蛋白。
重组HIV整合酶蛋白的最显着特征是其自缔合和形成寡聚体的倾向,这使得其结构难以研究。虽然可以获得部分晶体结构,但是全长蛋白质多年来一直在世界各地的研究人员中脱颖而出。
基于X射线和中子,SAXS和SANS的小角度散射技术在结构生物学和溶液生物物理学中的应用在过去15年中呈指数增长。它们提供丰富的信息,是我们用于了解分子结构的关键工具之一。
在这些方法中,X射线或实验中子的柱状光束指向大分子样品,并且散射强度作为散射角的函数绘制。
使用傅立叶变换分析,我们可以深入了解分子的形状和空间范围。然后可以将该信息直接与已知原子结构的分布进行比较,以确认溶液中的结构和组成。
但是,如果样品甚至被轻微污染或部分低聚,则对这些结果的解释会受到很大影响。这是SEC-MALS的表征和质量控制对小角度散射技术的发展和应用至关重要的地方,因为SAXS和SANS往往涉及昂贵的光束时间和行程。
SEC-MALS是使用小角度X射线散射成功研究HIV整合酶宿主因子相互作用的关键。它使我们能够筛选出许多突变和截短形式的重组整合酶复合物,因此我们可以获得目标复合物的高质量数据。在我们对整合酶和宿主晶状体上皮衍生生长因子(LEDGF)之间相互作用的研究中强调了这一点,LEDGF是病毒生命周期的重要组成部分。除了SEC-MALS之外,SEC-MALS对大型聚集体的存在比SEC-UV更敏感。在440kDa Lactocous Lactii Group II内含子蛋白-RNA复合物的情况下,它检测到低水平的大聚集体,不能被UV检测到。因此,我们进行了额外的纯化步骤,最终成功进行了SAXS测量并确定了高分辨率的低温EM结构。
同样,在我们2012年的双焦点研究中,SEC-MALS分析对于相关逆转录病毒整合酶蛋白-DNA复合物的表征至关重要。我们使用SEC-MALS证实,整合酶蛋白与病毒DNA结合,其化学计量为四个整合酶至两个DNA。SEC-MALS使我们能够优化缓冲条件并限制聚合。
SEC-MALS对您的研究成功至关重要吗?
绝对。在我们最近对HIV整合酶与称为ALLINIS的复杂新药物相互作用的结构研究中,SEC-MALS以及其他技术提供了首次获得全长蛋白质结构所需的突破。这反过来使我们能够研究由我们的新结构揭示的蛋白质 - 蛋白质相互作用。
ALLINI是HIV整合酶的有效变构抑制剂,目前正在临床试验中进行评估。通过研究LEDGF-整合酶相互作用的晶体结构来鉴定它们。很明显,小分子可以阻止这种相互作用,并在此过程的早期阻止HIV复制。
从我们在SEC-MALS的帮助下获得的结构鉴定了整合酶蛋白上的LEDGF结合位点,并且使用基于结构的设计开发了防止这种相互作用发生的分子。通过筛选破坏宿主因子LEDGF与整合酶结合的能力来选择潜在的候选药物。
您对ALLINIS的学习表现如何?
我们的研究集中在两个ALLINIS(GSK1264和GSKOO2)上。两种化合物共享连接取代的中心芳环系统的共同连接。并且X射线晶体学显示它们都以高亲和力结合整合酶催化结构域上的相同位点。
两种分子都具有有效的晚期复制效应,可显着破坏HIV颗粒组织并改变病毒颗粒形态的分布。这与它们催化HIV整合酶聚集的能力无关,而与温度和浓度无关。通过SEC-MALS监测这种聚集,并显示需要催化核心结构域和整合酶的C末端结构域。
我们想知道这些药物在结构层面是如何起作用的。什么是导致药物诱导的整合酶聚集的结构变化?
为了发现这一点,我们需要酶 - 药物复合物的结构。由于药物促进已经边缘可溶的蛋白质的聚集,这不利于获得有序的晶格用于通过x-ay晶体学分析。相反,我们开始使用多角度光散射,分析超速离心,小角度X射线散射(SAX)来表征复合物的许多点突变,以确定哪种形式的整合酶蛋白对ALLINI的反应较小。
使用SEC-MALS和沉降平衡分析,我们发现了仅作为二聚体存在的整合酶突变。即使在升高的药物浓度下,药物诱导的聚合也大大减弱。我们第一次能够结晶出与ALLINI复合的全长完整蛋白质。
我们能够使用分子置换研究模型来解决该结构,该模型用于先前确定的催化核心结构域和C末端结构域的结构。观察到广泛的蛋白质 - 蛋白质相互作用,其他整合酶形式未见。来自一个二聚体的C末端结构域到达相邻二聚体的核心结构域,非常类似于抓握球的手。
赋予对ALLINIS抗性的整合酶突变分为两类。它们或者直接破坏结合界面或扰乱药物定位以防止其结合。通过引入特定的整合酶突变,我们能够证实我们对这种药物稳定的蛋白质 - 蛋白质界面的新认识;再次,使用SEC-MALS结合其他技术确定寡聚体形式。
我们进行了一系列SEC-MALS研究,以进一步探索整合酶-ALLINI复合物的结构。正如我们新的晶体结构所强调的那样,最令人惊讶的发现是预期的聚合和后期复制效应。选择和设计ALLINI以中断LEDGF和整合酶之间的蛋白质 - 蛋白质相互作用,但我们的结果表明药物非常有效地稳定整合酶的开放聚合物。
这些结果共同为这类新药的药物设计方法提供了见解,刚刚进入临床试验阶段。
推荐内容
-
揭示了损害牛胚胎生产的机制
牛胚胎市场的长期障碍是卵母细胞中的脂质积累。研究人员现在已经描述了卵母细胞中脂质积累的前所未有的机制,这限制了牛胚胎体外生产的...
-
《大秦赋》赵姬私通是第几集 大秦赋赵姬和谁私通
现在很流行一个词,叫“下饭神剧”,顾名思义,就是喜欢在吃饭的时候看的电视剧。一般来形容一部剧非常的精彩,让人在吃饭的时候都难以...
-
心理咨询之婚恋观——白领不想结婚的理由_白领为什么不想结婚
如果一些还没谈过恋爱的男男女女们不知道该怎么处理异性人际关系可以看下过来人的一些建议,能帮助自己在爱情这条路上少走一些弯路。近...
-
心理咨询之婚恋观——【男人睡姿透露爱情秘密】男人睡姿透露他的
爱情和婚姻本身是美好的东西,但是因为每个人处理的方式不同导致结果有好有坏。很多人其实可以少看一些网络案例,毕竟感情这种事是很难...
-
心理咨询之婚恋观——【如何拥有幸福婚姻】拥有幸福婚姻的秘诀
感情这种事谁都说不准,与其自己一个人瞎猜不如看下经验者是如何应对这些问题的,多一个参考就能避免一些不必要的误会,了解的更多就会...
-
丙型肝炎病毒感染治愈后 高危门静脉高压症也将减轻
肝脏的丙型肝炎病毒感染会导致难以形成的疤痕组织形成。反过来,这会阻碍血液流经器官,导致门静脉高压。门脉高压是造成肝硬化大多数致...
-
心宅猎人原著小说结局是什么揭秘 最后谁死了谁活着
对于经常追剧的观众来说,电视剧是日常生活中不可或缺的一项元素。而近年来,无论是网剧还是电视剧,各种类型层出不穷。观众们有时也会...
-
让孩子胆大起来的妙招
一个人的性格跟他从小成长的环境分不开。父母亲的教育尤为重要,将会影响孩子的一生。如何让孩子胆大起来是父母们一直烦恼的问题,面对...
-
心理咨询之婚恋观——恋爱恐惧症怎么办_恋爱恐惧症解决方法
面对现在的社会压力,很多人选择先发展事业再决定谈恋爱结婚这件事。毕竟很多人都觉得爱情可遇不可求,不是说你努力去脱单就能脱单的,...
-
为何有七成人拿金钱衡量成功
【七成人拿金钱衡量成功】为何有七成人拿金钱衡量成功前言:心理疾病是现在特别流行的一种人体隐疾,因为很多人都没注意到。但是。如果...